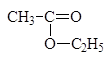Производные карбоновых кислот. Сложные эфиры
1. Ангидриды карбоновых кислот
Гидроксил карбоксильной группы способен при определенных условиях замещаться на другие атомы или группы атомов.
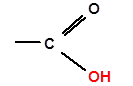
Ангидриды
В присутствии водоотнимающих средств, таких как оксид фосфора (V), гидроксил одной карбоновой кислоты замещается на остаток другой карбоновой кислоты:
2RCOOH ![]() (RCO)2O + Н2О
(RCO)2O + Н2О
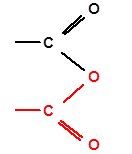
Ангидриды карбоновых кислот (RCO)2O – производные карбоновых кислот, представляющие собой продукт замещения гидроксила карбоксильной группы одной кислоты на остаток другой кислоты.
Малеиновый ангидрид:
Ангидриды карбоновых кислот более реакционноспособны, чем сами кислоты и сложные эфиры. Они легко вступают в реакции нуклеофильного замещения – например, гидролизуются:
(RCO)2О + H2O = 2RCOOH.
Галогенангидриды
При взаимодействии с галогенидами фосфора происходит замена гидроксила на атом галогена:
RCOOH + PCl5 = RCOCl + POCl3 + HCl
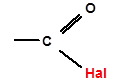
Галогенангидриды RCOНаl – производные карбоновых кислот, у которых гидроксил карбоксильной группы замещен на атом галогена.
Галогенангидриды еще реакционноспособнее ангидридов.
Амиды и нитрилы
Амиды можно получить аммонолизом хлорангидридов или ангидридов:
RCOCl + 2NH3 = RCONH2 + NH4Cl
или нагреванием аммониевых солей карбоновых кислот:
RCOONH4![]() RCONH2 + H2O.
RCONH2 + H2O.
Если нагревать амид дальше в присутствии Р2О5, то он превращается в нитрил:
RCONH2![]() RCN + H2O.
RCN + H2O.
Нитрил можно также получить, замещая гидроксил или атом галогена на цианогруппу. Гидролизом нитрилов в кислой среде получают кислоты:
RCN + 2H2O + HCl = RCOOH + NH4Cl
2. Сложные эфиры
В присутствии сильных неорганических кислот гидроксильная группа обратимо обменивается на остаток спирта:
RCOOH + R’OH ![]() RCOOR’ + H2O
RCOOR’ + H2O
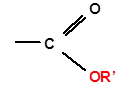
Сложные эфиры RCOOR’ – производные карбоновых кислот, у которых гидроксил карбоксильной группы замещен на остаток спирта.
3. Номенклатура сложных эфиров
|
|
||
|
этилацетат |
||
|
углеводородный заместитель |
+ |
кислотный остаток |
Названия по ИЮПАК выделены жирным шрифтом:
|
H–COO–C2H5 |
CH3–COO–CH3–CH3 |
CH2CH2–COO–C2H5 |
|
Этилформиат, этилметаноат; этиловый эфир муравьиной кислоты |
Метилацетат, метилэтаноат; метиловый эфир уксусной кислоты |
Этилбутират, этилбутаноат; этиловый эфир бутановой кислоты |
4. Физические свойства, запахи эфиров
Запахи эфиров:


Рис. 1.
Сложные эфиры нерастворимы в воде, но хорошо смешиваются со многими органическими веществами. Именно поэтому они используются как растворители для лаков и красок. Рис. 1. Этилацетат и метил ацетат – основа растворителя – жидкости для снятия лака с ногтей.
Температуры кипения сложных эфиров меньше, чем температуры кипения кислот и спиртов с близкой молярной массой. Почему? Сложные эфиры, в отличие от кислот и спиртов, не способны образовывать водородные связи между молекулами. Табл. 1.

Табл. 1. Сравнение температуры кипения эфиров
5. Способность к гидролизу эфиров
Главное химическое свойство сложных эфиров – способность к гидролизу:
H–COO–C2H5 + H2O ![]() H–COOH + C2H5OH;
H–COOH + C2H5OH;
CH3–COO–CH3 + NaOH ® CH3–COONa + CH3OH.
Подведение итога
Вы рассмотрели тему «Производные карбоновых кислот. Сложные эфиры». Благодаря этой теме, вы смогли познакомиться с производными карбоновых кислот. Также вы изучили самые важные функциональные производные карбоновых кислот – сложные эфиры. Рассмотрели их состав, некоторые свойства, формирование названий и сферы их применения в жизни.