Давление газа
1. Особенности молекулярного строения газов
Прежде чем непосредственно перейти к изучению давления газа, вспомним, какие особенности имеет расположение и движение молекул, из которых газ состоит.
Во-первых, молекулы газа движутся беспорядочно, хаотично.
Во-вторых, расстояния между молекулами достаточно большие по сравнению с размерами молекул.
В-третьих, вследствие большого расстояния между молекулами, силы притяжения между ними пренебрежимо малы, а силы отталкивания становятся заметными только при столкновениях молекул. Столкновения могут происходить как между самими молекулами, так и между молекулами и стенками сосуда (Рис. 1).
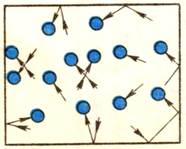
Рис. 1. Движение молекул газа в сосуде
Если взять воздушный шарик и немного его надуть, то он приобретет округлую форму, равномерно надуваясь со всех сторон (Рис. 2).

Рис. 2. Надутый шарик имеет округлую форму
Такая форма шарика объясняется тем, что молекулы газа оказывают давление не так, как молекулы твердых тел. Ведь молекулы газа движутся хаотично. Поэтому молекулы воздуха, которым наполнен шарик, ударяются о внутренние стенки оболочки шарика одинаково во всех направлениях. А значит, и давление воздуха не сосредотачивается на каких-то определенных участках оболочки, а равномерно распределяется по всей ее поверхности.
Итак, давление газа объясняется ударами его молекул о стенки сосуда, в котором находится газ.
2. Зависимость давления газа от объема
Убедимся в том, что молекулы газа действительно расположены достаточно далеко друг от друга, и поэтому газы хорошо сжимаемы.
Возьмем шприц и расположим его поршень приблизительно посередине цилиндра. Отверстие шприца соединим с трубкой, второй конец которой наглухо закрыт. Таким образом, некоторая порция воздуха будет заключена в цилиндре шприца под поршнем и в трубке (Рис. 3).

Рис. 3. В цилиндре под поршнем заключено некоторое количество воздуха
Теперь поставим на подвижный поршень шприца груз. Легко заметить, что поршень немного опустится. Это означает, что объем воздуха уменьшился (Рис. 4). Другими словами, газы (в нашем случае воздух) легко сжимаются. Таким образом, между молекулами газа имеются достаточно большие промежутки.

Рис. 4. Помещение груза на поршень вызывает уменьшение объема газа
С другой стороны, после установки груза поршень, немного опустившись, останавливается в новом положении равновесия. Это означает, что сила давления воздуха на поршень (направленная вверх) увеличивается и снова уравновешивает возросший вес поршня с грузом (направленный вниз). А поскольку площадь поршня при этом остается неизменной, мы приходим к важному заключению.
При уменьшении объема газа его давление увеличивается.
Будем помнить при этом, что масса газа и его температура в ходе опыта оставались неизменными.
Объяснить зависимость давления от объема можно следующим образом. При увеличении объема газа расстояние между его молекулами увеличивается. Каждой молекуле теперь нужно пройти большее расстояние от одного удара со стенкой сосуда до другого. Средняя скорость движения молекул остается неизменной (если температура газа не меняется). Следовательно, молекулы газа реже ударяются о стенки сосуда, а это приводит к уменьшению давления газа. И, наоборот, при уменьшении объема газа его молекулы чаще ударяются о стенки сосуда, и давление газа увеличивается (Рис. 5).
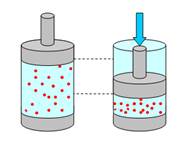
Рис. 5. При уменьшении объема газа расстояние между его молекулами уменьшается
3. Зависимость давления газа от температуры
В предыдущих опытах температура газа оставалась неизменной, и мы изучали изменение давления вследствие изменения объема газа. Теперь рассмотрим случай, когда объем газа остается постоянным, а температура газа изменяется. Масса при этом также остается неизменной. Создать такие условия можно, поместив некоторое количество газа в цилиндр с поршнем и закрепив поршень (Рис. 6).
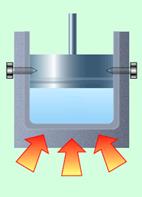
Рис. 6. Изменение температуры данной массы газа при неизменном объеме
Чем выше температура, тем быстрее движутся молекулы газа.
Следовательно,
- во-первых, чаще происходят удары молекул о стенки сосуда;
- во-вторых, средняя сила удара каждой молекулы о стенку становится больше.
Это приводит нас к еще одному важному заключению.
При увеличении температуры газа его давление увеличивается.
Будем помнить, что данное утверждение справедливо, если масса и объем газа в ходе изменения его температуры остаются неизменными.
4. Хранение и транспортировка газов
Зависимость давления газа от объема и температуры часто используется в технике и в быту. Если требуется перевезти значительное количество газа из одного места в другое, или когда газы необходимо длительно хранить, их помещают в специальные прочные металлические сосуды. Эти сосуды выдерживают высокие давления, поэтому с помощью специальных насосов (компрессоров) туда можно закачать значительные массы газа, которые в обычных условиях занимали бы в сотни раз больший объем (Рис. 7).

Рис. 7. Баллоны для хранения газов
Поскольку давление газов в баллонах даже при комнатной температуре очень велико, их ни в коем случае нельзя нагревать (например, держать под прямыми лучами солнца) или любым способом пытаться сделать в них отверстие даже после использования.
5. Заключение
Мы выяснили, что давление газов объясняется подвижностью молекул газа и ударами молекул о стенки сосудов, в которых газы заключены. Давление газа зависит от того, какой объем занимает данный газ, от его температуры и массы.
