Второй закон термодинамики. Необратимость тепловых процессов
1. Суть второго закона термодинамики
Существует несколько формулировок второго закона, но одна из самых понятных звучит так:
Теплота самопроизвольно передаётся только от более тёплого тела к более холодному.
Это означает, что:
-
горячее тело может нагревать холодное;
-
но холодное тело не может само нагреть горячее без внешнего воздействия.
Другая формулировка:
Невозможно полностью превратить теплоту в работу без других изменений в системе.
2. Необратимость тепловых процессов
Необратимые процессы — это процессы, которые не могут самопроизвольно идти в обратном направлении.
Примеры:
-
остывание горячего чая;
-
распространение запаха в комнате;
-
смешивание газов.
Если такие процессы произошли, вернуть систему в исходное состояние без внешней работы невозможно.
Наглядная схема направления теплопередачи


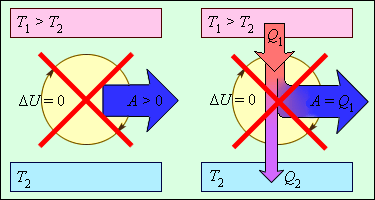

На схеме видно:
-
тепло всегда идёт от горячего тела к холодному;
-
обратный процесс невозможен сам по себе.
3. Почему процессы необратимы
Причины необратимости:
-
Разность температур
Тепло передаётся до тех пор, пока температуры не выровняются. -
Рассеивание энергии
Часть энергии превращается в менее полезные формы (например, внутреннюю энергию окружающей среды). -
Увеличение беспорядка (энтропии)
В природе процессы идут в сторону увеличения хаоса.
Например, молекулы газа сами равномерно распределяются по объёму, но не собираются обратно в одну часть.
4. Связь с тепловыми машинами
Второй закон объясняет, почему невозможно создать вечный двигатель второго рода — устройство, которое полностью превращает тепло в работу.
Любая тепловая машина:
-
получает тепло от нагревателя;
-
часть энергии превращает в работу;
-
остальное отдаёт холодильнику.
То есть всегда есть потери энергии.
5. Примеры из жизни
-
Чай остывает, но сам не нагревается обратно.
-
Лёд тает в комнате, но вода сама не превращается в лёд.
-
Двигатели автомобилей теряют часть энергии в виде тепла.
Все эти процессы подтверждают второй закон термодинамики.
6. Значение второго закона
Второй закон:
-
определяет направление процессов в природе;
-
показывает невозможность полного превращения энергии;
-
объясняет ограниченность эффективности машин.
Он играет важную роль в физике, технике и даже в понимании процессов во Вселенной.
Вопросы для самопроверки
-
Сформулируйте второй закон термодинамики.
-
В каком направлении передаётся теплота?
-
Что такое необратимый процесс?
-
Почему тепло не может самопроизвольно перейти от холодного тела к горячему?
-
Почему невозможно полностью превратить тепло в работу?
-
Приведите примеры необратимых процессов из жизни.
