Закон Авогадро. Состав молекул
Введение
Одной из важнейших задач химии является понимание того, как устроены молекулы веществ и каким образом можно определить их состав. На протяжении долгого времени ученые пытались объяснить, почему газы вступают в реакции в определённых соотношениях, и как можно установить количество частиц в веществе.
Решение этой задачи стало возможным благодаря работам итальянского ученого Амедео Авогадро, который в начале XIX века сформулировал один из фундаментальных законов химии — закон Авогадро.
Этот закон сыграл огромную роль в развитии атомно-молекулярного учения, помог определить состав молекул многих веществ и стал основой современной химии и физики.
В данной статье рассматриваются:
-
историческое развитие представлений о молекулах;
-
формулировка закона Авогадро;
-
понятие молекулы и молекулярного состава;
-
применение закона для определения состава молекул;
-
значение закона в химии и на практике.
История развития представлений о молекулах
Ранние представления о строении вещества
Ещё в древности ученые и философы пытались объяснить строение вещества.
-
Демокрит предположил, что все вещества состоят из мельчайших частиц — атомов.
-
Аристотель придерживался другой точки зрения, считая, что материя непрерывна.
Эти идеи долгое время оставались философскими и не имели экспериментального подтверждения.
Развитие атомной теории
В начале XIX века английский ученый Джон Дальтон разработал атомную теорию, согласно которой:
-
все вещества состоят из атомов;
-
атомы одного элемента одинаковы;
-
химические реакции — это перегруппировка атомов.
Однако теория Дальтона не объясняла некоторых закономерностей, наблюдаемых при взаимодействии газов.
Открытие закона Авогадро
В 1811 году Амедео Авогадро предложил гипотезу, которая позже получила название закона Авогадро.
Формулировка закона
В равных объемах различных газов при одинаковых температуре и давлении содержится одинаковое число молекул.
Этот закон позволил объяснить многие закономерности химических реакций газов.
Значение закона Авогадро
Закон Авогадро позволил:
-
различать атомы и молекулы;
-
определить состав молекул газов;
-
объяснить соотношения объемов газов в реакциях;
-
рассчитать количество частиц вещества.
Он стал важной частью молекулярно-кинетической теории.
Понятие молекулы
Молекула — это наименьшая частица вещества, сохраняющая его химические свойства.
Молекулы могут состоять:
-
из одного атома;
-
из нескольких атомов одного элемента;
-
из атомов разных элементов.
Состав молекул
Состав молекулы определяется:
-
видом атомов;
-
числом атомов;
-
порядком их соединения.
Примеры молекул
| Вещество | Формула | Состав |
|---|---|---|
| водород | H₂ | 2 атома водорода |
| кислород | O₂ | 2 атома кислорода |
| вода | H₂O | 2 H + 1 O |
| углекислый газ | CO₂ | 1 C + 2 O |
| метан | CH₄ | 1 C + 4 H |
Как закон Авогадро помогает определить состав молекул
До открытия закона было трудно объяснить, почему газы реагируют в определённых объемных соотношениях.
Например:
2 объема водорода + 1 объем кислорода → 2 объема воды (пара)
Закон Авогадро объясняет это следующим образом:
-
одинаковые объемы содержат одинаковое число молекул;
-
следовательно, реакция происходит между молекулами.
Пример определения состава молекулы воды
Рассмотрим реакцию образования воды:
2H₂ + O₂ → 2H₂O
Это означает:
-
две молекулы водорода;
-
одна молекула кислорода;
-
образуются две молекулы воды.
Из этого следует, что:
-
молекула водорода содержит два атома H;
-
молекула кислорода содержит два атома O.
Число Авогадро
Позже было установлено количество частиц в одном моле вещества.
Это число называется числом Авогадро:
6,02 × 10²³ частиц
Это означает, что:
-
в 1 моле любого вещества содержится одинаковое число частиц.
Понятие моля
Моль — это количество вещества, содержащее число частиц, равное числу Авогадро.
Например:
-
1 моль водорода содержит 6,02 × 10²³ молекул;
-
1 моль кислорода содержит столько же молекул.
Объем моля газа
При нормальных условиях:
1 моль газа занимает объем 22,4 литра.
Это называется молярный объем газа.
Применение закона Авогадро
1. Определение молекулярных формул
Закон позволяет определить состав молекул веществ.
2. Расчёты в химии
Используется при решении задач:
-
на количество вещества;
-
на объем газов;
-
на состав веществ.
3. Физика и термодинамика
Используется при изучении газовых законов.
4. Промышленность
Применяется при расчетах газовых процессов.
Закон Авогадро и газовые реакции
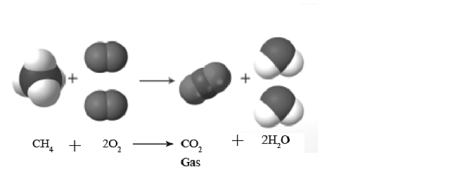
Пример реакции:
N₂ + 3H₂ → 2NH₃
Это означает:
-
1 объем азота;
-
3 объема водорода;
-
2 объема аммиака.
Такие соотношения объясняются законом Авогадро.
Значение закона для науки
Закон Авогадро стал важнейшим шагом в развитии химии.
Он помог:
-
подтвердить существование молекул;
-
определить молекулярные массы;
-
объяснить газовые реакции.
Современное значение закона
Сегодня закон используется в:
-
химии;
-
физике;
-
материаловедении;
-
биохимии;
-
экологии.
Он является фундаментом многих научных расчетов.
Вопросы для самопроверки
-
Кто сформулировал закон Авогадро?
-
Как формулируется закон Авогадро?
-
Что называется молекулой?
-
Что показывает химическая формула?
-
Что такое число Авогадро?
-
Почему закон Авогадро применим только к газам?
-
Как закон помогает определить состав молекул?
-
Что такое моль вещества?
-
Чему равен молярный объем газа?
-
Как связаны молекулы и химические реакции?
-
Определите состав молекулы воды по химической формуле.
-
Сколько молекул содержится в 1 моле вещества?
-
Почему одинаковые объемы газов содержат одинаковое число молекул?
-
Запишите уравнение реакции образования воды.
-
Приведите примеры веществ, молекулы которых состоят из одинаковых атомов.
