Валентность химических элементов
1. Понятие «валентность»
Состав большинства веществ постоянен. Например, молекула воды всегда содержит 2 атома водорода и 1 атом кислорода – Н2О. Возникает вопрос: почему вещества имеют постоянный состав?
Проанализируем состав предложенных веществ: Н2О, NaH, NH3, CH4, HCl. Все они состоят из атомов двух химических элементов, один из которых водород. На один атом химического элемента может приходиться 1,2,3,4 атома водорода. Но ни в одном веществе не будет на один атом водорода приходиться несколько атомов другого химического элемента. Таким образом, атом водорода может присоединять к себе минимальное количество атомов другого элемента, а точнее, только один.
Свойство атомов химического элемента присоединять к себе определенное число атомов других элементов называется валентностью.
2. Значения валентности химических элементов
Некоторые химические элементы имеют постоянные значения валентности (например, водород(I) и кислород(II)), другие могут проявлять несколько значений валентности (например, железо(II,III), сера(II,IV,VI), углерод(II,IV)), их называют элементами с переменной валентностью. Значения валентности некоторых химических элементов приведены в учебнике.
3. Графические формулы веществ
Зная валентности химических элементов, можно объяснить, почему вещество имеет именно такую химическую формулу. Например, формула воды H2O. Обозначим валентные возможности химического элемента с помощью черточек. Водород имеет валентность I, а кислород – II: Н- и -О-. Каждый атом может полностью использовать свои валентные возможности, если на один атом кислорода будет приходиться два атома водорода. Последовательность соединения атомов в молекуле воды можно представить в виде формулы: Н-О-Н.
Формула, в которой показана последовательность соединения атомов в молекуле, называется графической (или структурной).
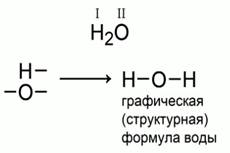
Рис. 1. Графическая формула воды
4. Определение валентности элемента по химической формуле вещества
Зная формулу вещества, состоящего из атомов двух химических элементов, и валентность одного из них, можно определить валентность другого элемента.
Пример 1. Определим валентность углерода в веществе СН4. Зная, что валентность водорода всегда равна I, а углерод присоединил к себе 4 атома водорода, можно утверждать, что валентность углерода равна IV. Валентность атомов обозначается римской цифрой над знаком элемента: 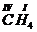 .
.
Пример 2. Определим валентность фосфорав соединении Р2О5. Для этого необходимо выполнить следующие действия:
1. над знаком кислорода записать значение его валентности – II (кислород имеет постоянное значение валентности);
2. умножив валентность кислорода на число атомов кислорода в молекуле, найти общее число единиц валентности – 2·5=10;
3. разделить полученное общее число единиц валентностей на число атомов фосфора в молекуле – 10:2=5.
Таким образом, валентность фосфора в данном соединении равна V – 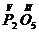 .
.
