Соотношение неопределенностей Гейзенберга. Два пути развития квантовой механики
1. Соотношение неопределённостей
Основная формула:
где:
— неопределённость координаты;
— неопределённость импульса;
— постоянная Планка.
Это означает:
нельзя одновременно точно знать положение и импульс частицы.
2. Физический смысл
-
Чем точнее измеряем координату → тем хуже знаем импульс;
-
Чем точнее импульс → тем больше неопределённость положения.
Это не ошибка приборов, а свойство природы.
Наглядная схема принципа неопределённости
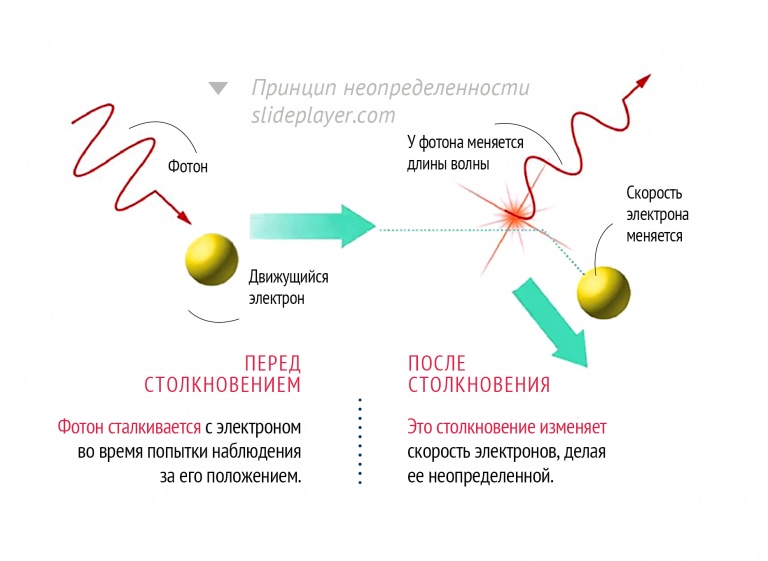
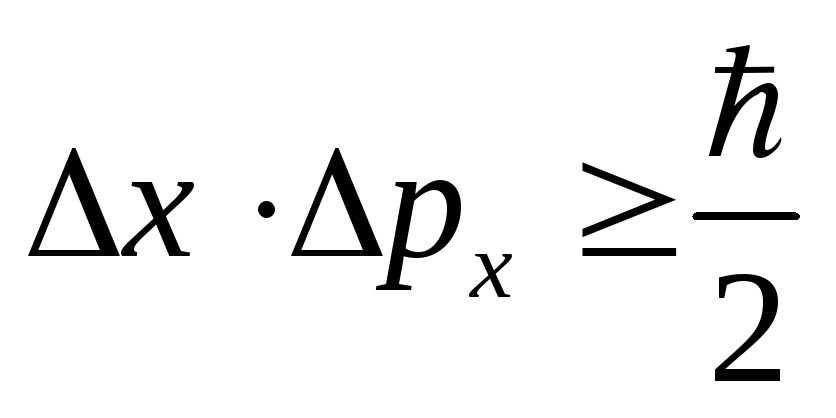

3. Причина возникновения
Связана с волновой природой частиц:
-
частица описывается волной;
-
волна не может быть строго локализована;
-
короткая волна → большой разброс импульсов.
Это следствие корпускулярно-волнового дуализма.
4. Примеры
-
Электрон в атоме не движется по чёткой орбите;
-
Нельзя указать точную траекторию частицы;
-
Возможны только вероятности нахождения.
5. Два пути развития квантовой механики
После открытия квантовых законов сформировались два подхода.
1) Волновая механика
Создатель — Эрвин Шрёдингер.
Основная идея:
-
частица описывается волновой функцией (\psi);
-
состояние системы определяется уравнением Шрёдингера;
-
результат — вероятность нахождения частицы.
2) Матричная механика
Создатели:
-
Вернер Гейзенберг
-
Макс Борн
-
Паскуаль Йордан
Основная идея:
-
физические величины описываются матрицами;
-
используются вероятностные переходы;
-
нет привычных траекторий.
Наглядная схема двух подходов

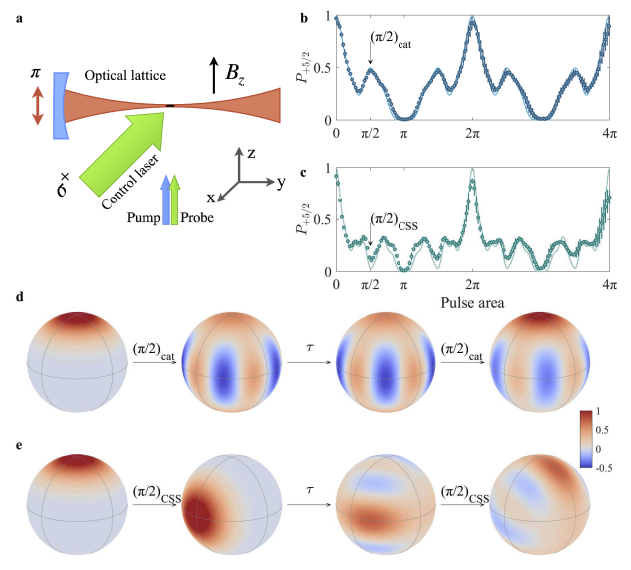

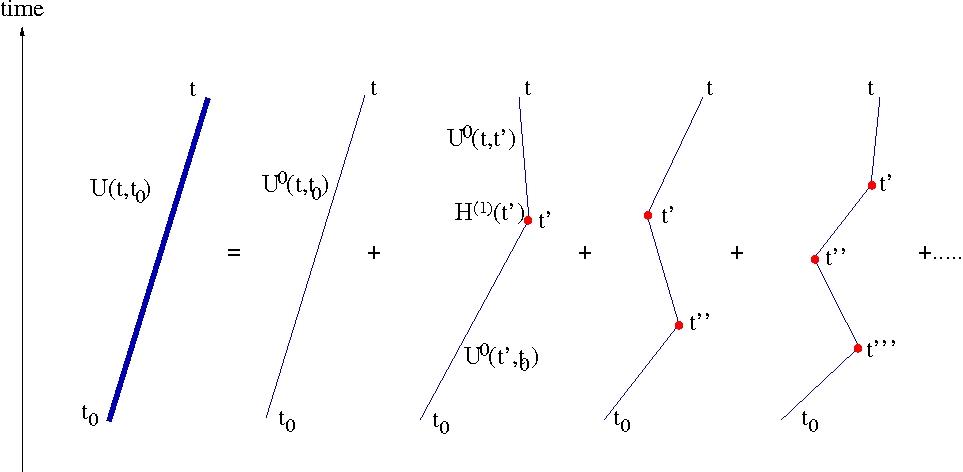
6. Единство теорий
Позже выяснилось:
обе теории эквивалентны и описывают одни и те же явления.
Они просто используют разные математические методы.
7. Значение принципа Гейзенберга
-
показывает границы измерений;
-
объясняет устойчивость атома;
-
лежит в основе квантовой физики;
-
используется в современных технологиях.
8. Итоги
-
В микромире нет точных траекторий;
-
Возможны только вероятности;
-
Квантовая механика имеет два подхода;
-
Принцип неопределённости — фундаментальный закон природы.
Вопросы для самопроверки
-
Запишите соотношение неопределённостей.
-
Почему нельзя точно измерить координату и импульс?
-
Является ли это ограничением приборов?
-
С чем связано появление неопределённости?
-
Кто создал волновую механику?
-
В чём суть матричной механики?
-
Чем отличаются эти подходы?
-
Почему они считаются эквивалентными?
