Относительная молярная и молекулярная массы вещества. Молярный объем вещества
Введение
Химия изучает состав веществ, их строение, свойства и превращения. Для того чтобы описывать вещества количественно, химики используют различные физические и химические величины. Среди них особое место занимают относительная молекулярная масса, молярная масса и молярный объём вещества. Эти понятия позволяют проводить расчёты в химических реакциях, определять состав веществ, устанавливать соотношения между массой, количеством вещества и объёмом газов.
Любое вещество состоит из мельчайших частиц — атомов, молекул или ионов. Чтобы понимать, сколько именно частиц участвует в химической реакции, была введена специальная величина — количество вещества, измеряемое в молях. Один моль вещества содержит строго определённое число частиц, называемое числом Авогадро.
Понятия молекулярной массы и молярной массы тесно связаны между собой. Относительная молекулярная масса показывает, насколько молекула одного вещества тяжелее условной атомной единицы массы. Молярная масса показывает массу одного моля вещества. А молярный объём определяет объём, который занимает один моль газа при определённых условиях.
Эти величины являются основой для решения многих задач в химии, поэтому их понимание чрезвычайно важно для изучения предмета.
Понятие молекулы вещества
Большинство веществ состоит из молекул. Молекула — это наименьшая частица вещества, которая сохраняет его химические свойства.
Молекулы образуются из атомов химических элементов, соединённых между собой химическими связями. Например:
-
молекула воды состоит из двух атомов водорода и одного атома кислорода
-
молекула углекислого газа состоит из одного атома углерода и двух атомов кислорода
-
молекула аммиака состоит из одного атома азота и трёх атомов водорода
Состав молекулы записывается с помощью химической формулы.
Примеры формул:
| Вещество | Формула |
|---|---|
| Вода | H₂O |
| Углекислый газ | CO₂ |
| Аммиак | NH₃ |
| Метан | CH₄ |
Для того чтобы сравнивать массы различных молекул, была введена величина относительной молекулярной массы.
Относительная молекулярная масса вещества
Относительная молекулярная масса — это число, показывающее, во сколько раз масса молекулы данного вещества больше 1/12 массы атома углерода-12.
Обозначается она:
Mr
где
M — молекулярная
r — относительная
Относительная молекулярная масса определяется как сумма относительных атомных масс всех атомов, входящих в состав молекулы.
Иначе говоря:
Mr вещества = сумма Ar всех атомов в формуле
где
Ar — относительная атомная масса элемента.
Расчёт относительной молекулярной массы
Рассмотрим несколько примеров.
Пример 1. Вода
Формула воды: H₂O
Mr(H₂O) = 2 × Ar(H) + Ar(O)
Ar(H) = 1
Ar(O) = 16
Mr(H₂O) = 2 × 1 + 16 = 18
Пример 2. Углекислый газ
Формула: CO₂
Mr(CO₂) = Ar(C) + 2 × Ar(O)
Ar(C) = 12
Ar(O) = 16
Mr(CO₂) = 12 + 2 × 16 = 44
Пример 3. Аммиак
Формула: NH₃
Mr(NH₃) = Ar(N) + 3 × Ar(H)
Ar(N) = 14
Ar(H) = 1
Mr(NH₃) = 14 + 3 × 1 = 17
Пример 4. Метан
Формула: CH₄
Mr(CH₄) = Ar(C) + 4 × Ar(H)
Mr(CH₄) = 12 + 4 × 1 = 16
Таким образом, относительная молекулярная масса является безразмерной величиной и используется для сравнения масс молекул различных веществ.
Понятие количества вещества

Для описания количества частиц вещества используется физическая величина количество вещества.
Она обозначается буквой:
n
Единица измерения — моль.
Один моль вещества содержит 6,02 × 10²³ частиц.
Это число называется числом Авогадро.
Один моль может содержать:
-
атомы
-
молекулы
-
ионы
Например:
1 моль воды содержит
6,02 × 10²³ молекул воды.
1 моль кислорода содержит
6,02 × 10²³ молекул O₂.
Молярная масса вещества
Молярная масса — это масса одного моля вещества.
Обозначается:
M
Единица измерения:
г/моль
Молярная масса численно равна относительной молекулярной массе вещества.
Например:
| Вещество | Mr | M |
|---|---|---|
| H₂O | 18 | 18 г/моль |
| CO₂ | 44 | 44 г/моль |
| NH₃ | 17 | 17 г/моль |
| CH₄ | 16 | 16 г/моль |
Связь массы и количества вещества
Масса вещества связана с количеством вещества формулой:
n = m / M
где
n — количество вещества (моль)
m — масса вещества (г)
M — молярная масса (г/моль)
Также можно записать:
m = n × M
Пример задачи
Определить количество вещества воды массой 36 г.
Молярная масса воды:
M(H₂O) = 18 г/моль
Используем формулу:
n = m / M
n = 36 / 18
n = 2 моль
Молярный объём вещества
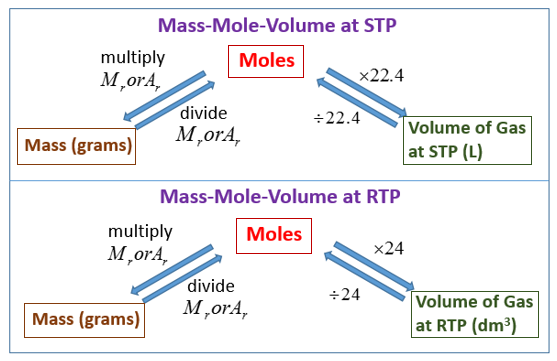
Для газов важной характеристикой является молярный объём.
Молярный объём — это объём, который занимает один моль газа при определённых условиях.
Обозначается:
Vm
Единица измерения:
л/моль
При нормальных условиях (0°C и 1 атмосфера) один моль любого газа занимает:
22,4 литра
Таким образом:
Vm = 22,4 л/моль
Это правило справедливо для всех газов.
Связь объёма и количества вещества
Для газов используется формула:
n = V / Vm
где
n — количество вещества
V — объём газа
Vm — молярный объём
Также можно записать:
V = n × Vm
Пример задачи
Найти объём 2 моль кислорода при нормальных условиях.
Vm = 22,4 л/моль
V = n × Vm
V = 2 × 22,4
V = 44,8 л
Примеры задач
Задача 1
Найти молярную массу углекислого газа.
Формула CO₂.
M = 12 + 2 × 16
M = 44 г/моль.
Задача 2
Сколько молей содержится в 44 г CO₂?
M = 44 г/моль.
n = m / M
n = 44 / 44
n = 1 моль.
Задача 3
Какой объём занимает 3 моль азота?
Vm = 22,4 л/моль.
V = n × Vm
V = 3 × 22,4
V = 67,2 л.
Значение этих понятий в химии
Понятия молекулярной массы, молярной массы и молярного объёма имеют огромное значение:
-
позволяют рассчитывать массы веществ;
-
помогают определять количество вещества;
-
используются при решении задач;
-
позволяют рассчитывать объёмы газов;
-
применяются в химических реакциях.
Эти величины широко используются в лабораторной практике, промышленности и научных исследованиях.
Применение в промышленности и науке
Эти понятия применяются во многих областях:
Химическая промышленность
Используются для расчёта количества реагентов и продуктов реакции.
Фармацевтика
Позволяют точно рассчитывать состав лекарственных препаратов.
Экология
Используются для определения концентрации газов в атмосфере.
Металлургия
Помогают рассчитывать количество реагентов при переработке руд.
Заключение
Относительная молекулярная масса, молярная масса и молярный объём вещества являются важнейшими понятиями химии. Они позволяют проводить количественные расчёты, определять состав веществ и устанавливать взаимосвязь между массой, количеством вещества и объёмом газов.
Относительная молекулярная масса показывает, насколько тяжела молекула вещества по сравнению с атомной единицей массы. Молярная масса показывает массу одного моля вещества. Молярный объём характеризует объём, который занимает один моль газа при нормальных условиях.
Понимание этих понятий необходимо для решения задач, проведения химических экспериментов и изучения химических процессов.
Вопросы для самопроверки
-
Что называется молекулой вещества?
-
Что показывает относительная молекулярная масса?
-
Как обозначается относительная молекулярная масса?
-
Как вычисляется относительная молекулярная масса вещества?
-
Что называется количеством вещества?
-
В каких единицах измеряется количество вещества?
-
Чему равно число Авогадро?
-
Что называется молярной массой вещества?
-
В каких единицах измеряется молярная масса?
-
Как связаны масса вещества и количество вещества?
-
Что называется молярным объёмом газа?
-
Чему равен молярный объём газа при нормальных условиях?
-
Как рассчитать объём газа через количество вещества?
-
Как определить количество вещества по массе?
-
Почему понятия молярной массы и молярного объёма важны в химии?
