Относительная атомная масса химических элементов
Введение
Химия как наука изучает вещества, их состав, свойства и превращения. Для того чтобы описывать и сравнивать различные вещества, химики используют специальные количественные характеристики. Одной из важнейших таких характеристик является относительная атомная масса химического элемента. Она позволяет определить, насколько тяжел атом одного элемента по сравнению с атомом другого.
Понятие относительной атомной массы играет фундаментальную роль в химии. Без него невозможно проводить расчёты в химических реакциях, определять состав соединений, вычислять молярные массы веществ и решать многие практические задачи. Именно поэтому данная тема изучается на начальных этапах курса химии и служит основой для дальнейшего понимания строения вещества.
Исторически понятие атомной массы появилось в процессе развития атомно-молекулярной теории. Ученые пытались понять, из чего состоят вещества, как взаимодействуют атомы и каким образом можно количественно описать эти процессы. Постепенно были разработаны методы измерения масс атомов, что позволило создать периодическую систему элементов и значительно продвинуть развитие химической науки.
В данной статье мы подробно рассмотрим понятие относительной атомной массы, историю её появления, способы определения, значение в химии, а также научимся использовать её при решении различных задач.
Понятие атомной массы
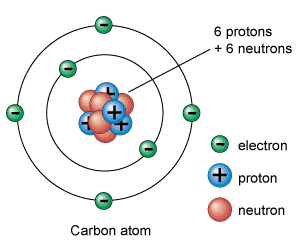
Каждый химический элемент состоит из мельчайших частиц — атомов. Атом имеет сложное строение: в центре находится ядро, состоящее из протонов и нейтронов, вокруг которого движутся электроны.
Масса атома определяется суммой масс частиц, входящих в его состав:
-
протонов
-
нейтронов
-
электронов
Однако масса электрона чрезвычайно мала по сравнению с массой протона и нейтрона, поэтому в большинстве химических расчётов ею пренебрегают.
Абсолютная масса атома очень мала. Например:
-
масса атома водорода ≈ 1,67 × 10⁻²⁷ кг
-
масса атома кислорода ≈ 2,66 × 10⁻²⁶ кг
Такие значения неудобно использовать в расчетах. Поэтому ученые ввели относительную атомную массу — величину, показывающую, во сколько раз масса атома данного элемента больше определённой условной единицы.
Понятие относительной атомной массы
Относительная атомная масса — это число, показывающее, во сколько раз средняя масса атома химического элемента больше 1/12 массы атома углерода-12.
Обозначается она символом:
Ar
где:
-
A — атомная
-
r — относительная
Таким образом:
Ar = масса атома элемента / (1/12 массы атома углерода-12)
Углерод-12 был выбран в качестве стандарта, потому что:
-
этот изотоп устойчив;
-
он широко распространён в природе;
-
его атом удобно использовать как эталон.
Относительная атомная масса — безразмерная величина, так как она представляет собой отношение двух масс.
Например:
-
Ar(H) ≈ 1
-
Ar(O) ≈ 16
-
Ar(Na) ≈ 23
-
Ar(Fe) ≈ 56
Это означает, что атом кислорода примерно в 16 раз тяжелее атома водорода, а атом железа — примерно в 56 раз тяжелее.
История открытия атомных масс
Развитие представлений об атомных массах происходило постепенно. Огромный вклад в эту область внесли многие ученые.
Джон Дальтон
Английский ученый Джон Дальтон в начале XIX века предложил атомную теорию строения вещества. Он предположил, что:
-
все вещества состоят из атомов;
-
атомы различных элементов имеют различную массу;
-
атомы соединяются в определённых соотношениях.
Дальтон составил первую таблицу атомных масс элементов.
Амедео Авогадро
Итальянский ученый Амедео Авогадро сформулировал закон, согласно которому одинаковые объемы газов при одинаковых условиях содержат одинаковое число молекул. Это позволило точнее определять массы атомов и молекул.
Дмитрий Менделеев
Русский ученый Дмитрий Иванович Менделеев создал периодическую систему элементов. Он расположил элементы в таблице в порядке увеличения их атомных масс, обнаружив периодичность свойств.
Позднее было установлено, что правильнее располагать элементы по атомному номеру, однако атомная масса продолжает оставаться важнейшей характеристикой элемента.
Изотопы и относительная атомная масса

Атомы одного и того же элемента могут иметь различное число нейтронов. Такие разновидности атомов называются изотопами.
Например, у углерода есть несколько изотопов:
-
углерод-12
-
углерод-13
-
углерод-14
Они имеют одинаковое число протонов, но различное число нейтронов.
В природе элементы обычно представлены смесью изотопов. Поэтому относительная атомная масса элемента — это среднее значение масс всех его изотопов с учетом их распространенности.
Например:
Ar(Cl) = 35,5
Это означает, что в природе хлор состоит из смеси изотопов с массами около 35 и 37.
Относительная атомная масса и периодическая система

Относительная атомная масса указана в периодической таблице элементов.
Каждая клетка таблицы содержит:
-
символ элемента
-
порядковый номер
-
относительную атомную массу
Например:
| Элемент | Символ | Ar |
|---|---|---|
| Водород | H | 1 |
| Углерод | C | 12 |
| Кислород | O | 16 |
| Натрий | Na | 23 |
| Железо | Fe | 56 |
По этим значениям можно проводить различные химические расчеты.
Использование относительной атомной массы
Относительная атомная масса используется в различных областях химии:
1. Определение молекулярной массы
Молекулярная масса вещества равна сумме атомных масс всех атомов, входящих в состав молекулы.
Например:
H₂O
Mr(H₂O) = 2 × Ar(H) + Ar(O)
Mr(H₂O) = 2 × 1 + 16 = 18
2. Определение молярной массы
Молярная масса вещества численно равна его относительной молекулярной массе.
Например:
M(H₂O) = 18 г/моль
3. Расчёт состава вещества
Относительные атомные массы позволяют определить:
-
массовую долю элементов
-
формулу вещества
-
количество вещества
Примеры расчетов
Пример 1
Найти относительную молекулярную массу CO₂.
Mr(CO₂) = Ar(C) + 2 × Ar(O)
Mr(CO₂) = 12 + 2 × 16 = 44
Пример 2
Найти относительную молекулярную массу NH₃.
Mr(NH₃) = Ar(N) + 3 × Ar(H)
Mr(NH₃) = 14 + 3 × 1 = 17
Пример 3
Найти молекулярную массу H₂SO₄.
Mr(H₂SO₄) = 2 × Ar(H) + Ar(S) + 4 × Ar(O)
Mr(H₂SO₄) = 2 × 1 + 32 + 4 × 16
Mr(H₂SO₄) = 98
Значение атомных масс в химии
Относительная атомная масса имеет огромное значение:
-
Позволяет сравнивать атомы различных элементов.
-
Используется при составлении химических формул.
-
Помогает проводить количественные расчёты.
-
Позволяет определять состав соединений.
-
Используется в химическом анализе.
Без этого понятия невозможно развитие современной химии.
Применение в науке и промышленности
Относительная атомная масса используется:
-
в химической промышленности;
-
в фармацевтике;
-
в металлургии;
-
в экологических исследованиях;
-
в медицине.
Например, при производстве лекарств необходимо точно знать массу атомов элементов, входящих в состав молекул препарата.
Заключение
Относительная атомная масса является одной из фундаментальных характеристик химических элементов. Она показывает, насколько тяжел атом одного элемента по сравнению с условной единицей массы — одной двенадцатой частью массы атома углерода-12.
История развития этого понятия связана с именами многих выдающихся ученых — Дальтона, Авогадро, Менделеева и других. Благодаря их исследованиям стало возможным точно измерять массы атомов и использовать эти данные для научных и практических целей.
Относительная атомная масса используется при расчётах молекулярных и молярных масс веществ, определении состава соединений, изучении химических реакций и во многих других областях науки и промышленности.
Понимание этого понятия является важным этапом в изучении химии и позволяет лучше разобраться в строении вещества и закономерностях химических процессов.
Вопросы для самопроверки
-
Что называется атомом?
-
Какие частицы входят в состав атома?
-
Почему абсолютные массы атомов неудобно использовать в расчетах?
-
Что называется относительной атомной массой?
-
Как обозначается относительная атомная масса?
-
Какой атом выбран в качестве стандарта атомной массы?
-
Что такое изотопы?
-
Почему относительная атомная масса часто имеет дробное значение?
-
Где можно найти значения относительных атомных масс элементов?
-
Как рассчитать молекулярную массу вещества?
-
Чему равна относительная молекулярная масса воды?
-
Чему равна относительная молекулярная масса углекислого газа?
-
Какую роль играет относительная атомная масса в химии?
-
Какие ученые внесли вклад в развитие атомно-молекулярной теории?
-
В каких областях науки и промышленности используется относительная атомная масса?
