Электронная оболочка атома
Электронная оболочка атома
Введение
Понимание строения электронной оболочки атома является ключом к объяснению химических свойств элементов, природы химических связей и закономерностей периодической системы. Электроны, находящиеся вокруг атомного ядра, определяют реакционную способность вещества, его способность образовывать соединения и физико-химические свойства.
Современные представления об электронной оболочке сформировались благодаря развитию квантовой механики, спектроскопии и теории строения атома. В данной статье подробно рассматриваются структура электронной оболочки, энергетические уровни и подуровни, орбитали, принципы заполнения электронов и их роль в химических свойствах элементов.
1. Общие представления об электронной оболочке атома
Атом состоит из положительно заряженного ядра и электронной оболочки, в которой находятся электроны.
Основные характеристики электронов:
-
отрицательный электрический заряд;
-
чрезвычайно малая масса;
-
волново-частичные свойства;
-
участие в химических взаимодействиях.
Электронная оболочка занимает практически весь объём атома.
2. История формирования представлений об электронной оболочке
2.1 Планетарная модель
Эрнест Резерфорд предположил, что электроны вращаются вокруг ядра подобно планетам.
Однако модель не объясняла устойчивость атома.
2.2 Квантовая модель
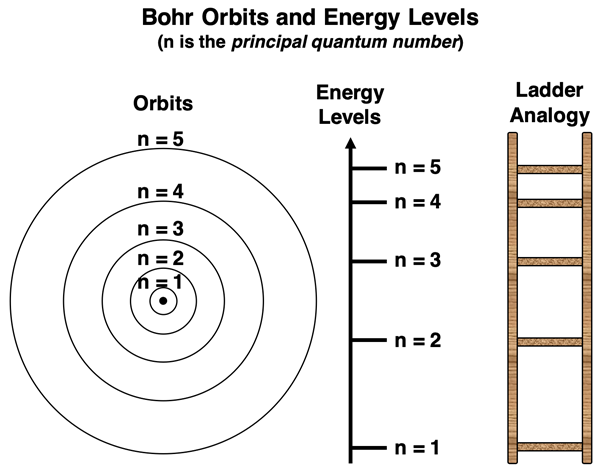
Нильс Бор предложил идею стационарных орбит и энергетических уровней.
Позже квантовая механика показала, что электроны находятся в областях вероятного пребывания.
3. Энергетические уровни электронной оболочки
Электроны располагаются вокруг ядра на определённых энергетических уровнях.
Обозначения уровней:
| Уровень | n | Оболочка |
|---|---|---|
| 1 | 1 | K |
| 2 | 2 | L |
| 3 | 3 | M |
| 4 | 4 | N |
Чем дальше уровень от ядра, тем выше энергия электрона.
Максимальное число электронов
Определяется формулой:
2n²
Примеры:
-
1 уровень — 2 электрона
-
2 уровень — 8 электронов
-
3 уровень — 18 электронов
4. Электронные подуровни
Каждый энергетический уровень состоит из подуровней.
| Подуровень | Обозначение | Форма |
|---|---|---|
| s | sharp | сферическая |
| p | principal | гантелеобразная |
| d | diffuse | сложная |
| f | fundamental | сложная |
Вместимость подуровней
-
s — 2 электрона
-
p — 6 электронов
-
d — 10 электронов
-
f — 14 электронов
5. Атомные орбитали
Орбиталь — область пространства, где вероятность нахождения электрона максимальна.
Типы орбиталей:
s-орбиталь
Сферическая форма.
p-орбитали
Три взаимно перпендикулярные орбитали.
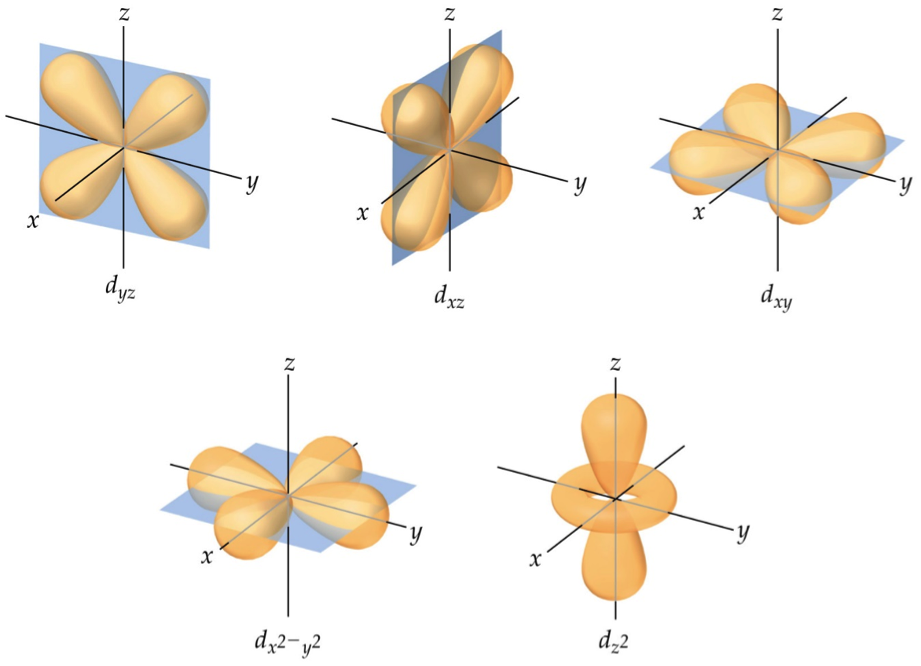
d-орбитали
Пять орбиталей сложной формы.
f-орбитали
Сложные многолепестковые формы.
6. Квантовые числа
Положение электрона в атоме описывается квантовыми числами.
Главное квантовое число (n)
Определяет энергетический уровень.
Орбитальное квантовое число (l)
Определяет форму орбитали.
Магнитное квантовое число (m)
Определяет ориентацию орбитали.
Спиновое квантовое число (s)
Определяет направление вращения электрона.
7. Принципы заполнения электронной оболочки
7.1 Принцип минимальной энергии (правило Клечковского)
Электроны заполняют орбитали в порядке возрастания энергии:
1s → 2s → 2p → 3s → 3p → 4s → 3d → 4p …
7.2 Принцип Паули
На одной орбитали может находиться не более двух электронов с противоположными спинами.
7.3 Правило Хунда
Электроны сначала занимают свободные орбитали по одному.
8. Электронные конфигурации атомов
Электронная конфигурация показывает распределение электронов по орбиталям.
Примеры:
Водород: 1s¹
Гелий: 1s²
Углерод: 1s² 2s² 2p²
Неон: 1s² 2s² 2p⁶
Электронная конфигурация определяет положение элемента в периодической системе.
9. Валентные электроны
Валентные электроны — электроны внешнего уровня.
Они:
-
участвуют в образовании химических связей;
-
определяют химическую активность;
-
влияют на свойства элемента.
Например:
-
натрий — 1 валентный электрон;
-
магний — 2;
-
кислород — 6.
10. Возбуждённые состояния атома
При поглощении энергии электрон переходит на более высокий уровень.
Это состояние называется возбуждённым.
При возвращении электрона выделяется энергия в виде света.
Это явление объясняет:
-
спектры излучения;
-
свечение газов;
-
работу лазеров.
11. Ионизация атома
Ионизация — процесс потери или присоединения электронов.
Катионы
Образуются при потере электронов.
Анионы
Образуются при присоединении электронов.
Ионы играют важную роль в химических реакциях.
12. Связь электронной оболочки с периодической системой

Строение электронной оболочки определяет положение элемента в таблице.
Периоды
Определяются числом энергетических уровней.
Группы
Определяются числом валентных электронов.
Элементы одной группы имеют сходные химические свойства.
13. Электронная оболочка и химическая связь
Электронная оболочка играет решающую роль в образовании связей.
Типы химических связей:
Ковалентная — общие электронные пары.
Ионная — передача электронов.
Металлическая — «электронный газ».
14. Электроотрицательность и радиус атома
Электронная оболочка влияет на:
Радиус атома
Увеличивается вниз группы.
Электроотрицательность
Увеличивается слева направо.
Эти свойства определяют химическую активность элементов.
15. Спектры атомов
Электронные переходы между уровнями сопровождаются излучением.
Каждый элемент имеет уникальный спектр.
Спектральный анализ используется:
-
в химии;
-
астрономии;
-
криминалистике.
16. Современные методы изучения электронной оболочки
Учёные используют:
-
спектроскопию;
-
рентгеноструктурный анализ;
-
электронную микроскопию;
-
квантовые расчёты.
Эти методы позволяют изучать электронную структуру атомов и молекул.
17. Значение электронной оболочки для химии
Строение электронной оболочки определяет:
-
химическую активность;
-
валентность;
-
способность образовывать соединения;
-
физические свойства веществ.
Понимание электронной структуры необходимо для разработки новых материалов, лекарств и технологий.
Заключение
Электронная оболочка атома — это сложная система, определяющая химические свойства элементов и их способность взаимодействовать друг с другом. Современная квантово-механическая модель описывает электроны как частицы, находящиеся в областях вероятного пребывания — орбиталях.
Изучение электронной оболочки позволяет понять закономерности периодической системы, природу химических связей и механизмы химических реакций. Это знание лежит в основе современной химии, материаловедения, нанотехнологий и фармацевтики.
Вопросы для самопроверки
-
Что такое электронная оболочка атома?
-
Какой заряд имеет электрон?
-
Что такое энергетический уровень?
-
Сколько электронов помещается на s-подуровне?
-
Что такое орбиталь?
-
Чем отличаются s- и p-орбитали?
-
Что определяет главное квантовое число?
-
Сформулируйте принцип Паули.
-
Что такое валентные электроны?
-
Как электроны участвуют в образовании химических связей?
-
Почему электроны располагаются по уровням?
-
Как электронная оболочка определяет положение элемента в таблице?
-
Чем отличается возбуждённое состояние атома?
-
Что происходит при ионизации?
-
Почему элементы одной группы имеют сходные свойства?
