Трудности планетарной модели атома Резерфорда. Модель водородоподобного атома Н. Бора
В начале XX века строение атома активно изучалось. После экспериментов по рассеянию частиц Эрнест Резерфорд предложил планетарную модель атома, согласно которой электроны движутся вокруг ядра, как планеты вокруг Солнца. Однако эта модель имела серьёзные проблемы.
1. Планетарная модель Резерфорда
Согласно модели:
-
атом состоит из маленького положительного ядра;
-
вокруг ядра движутся электроны;
-
большая часть объёма атома — пустота.
Модель хорошо объяснила результаты экспериментов.
Наглядная схема модели Резерфорда
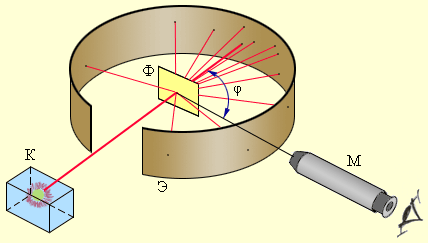


2. Трудности модели Резерфорда
Несмотря на успехи, возникли серьёзные противоречия:
1. Проблема устойчивости атома
По законам классической физики движущийся электрон должен излучать энергию и:
-
терять скорость;
-
падать на ядро.
Атом должен разрушиться, но этого не происходит.
2. Непрерывный спектр излучения
Классическая теория предсказывает:
-
непрерывное излучение энергии.
Но в опытах наблюдаются линейчатые спектры.
3. Отсутствие объяснения уровней энергии
Модель не объясняет:
-
почему электроны могут находиться только на определённых расстояниях от ядра.
3. Модель атома Нильс Бор
В 1913 году Бор предложил новую модель, устраняющую недостатки модели Резерфорда.
Основные постулаты Бора:
-
Электрон движется по стационарным орбитам и не излучает энергию.
-
Излучение происходит только при переходе между орбитами.
-
Энергия электрона принимает дискретные значения.
Наглядная схема модели Бора


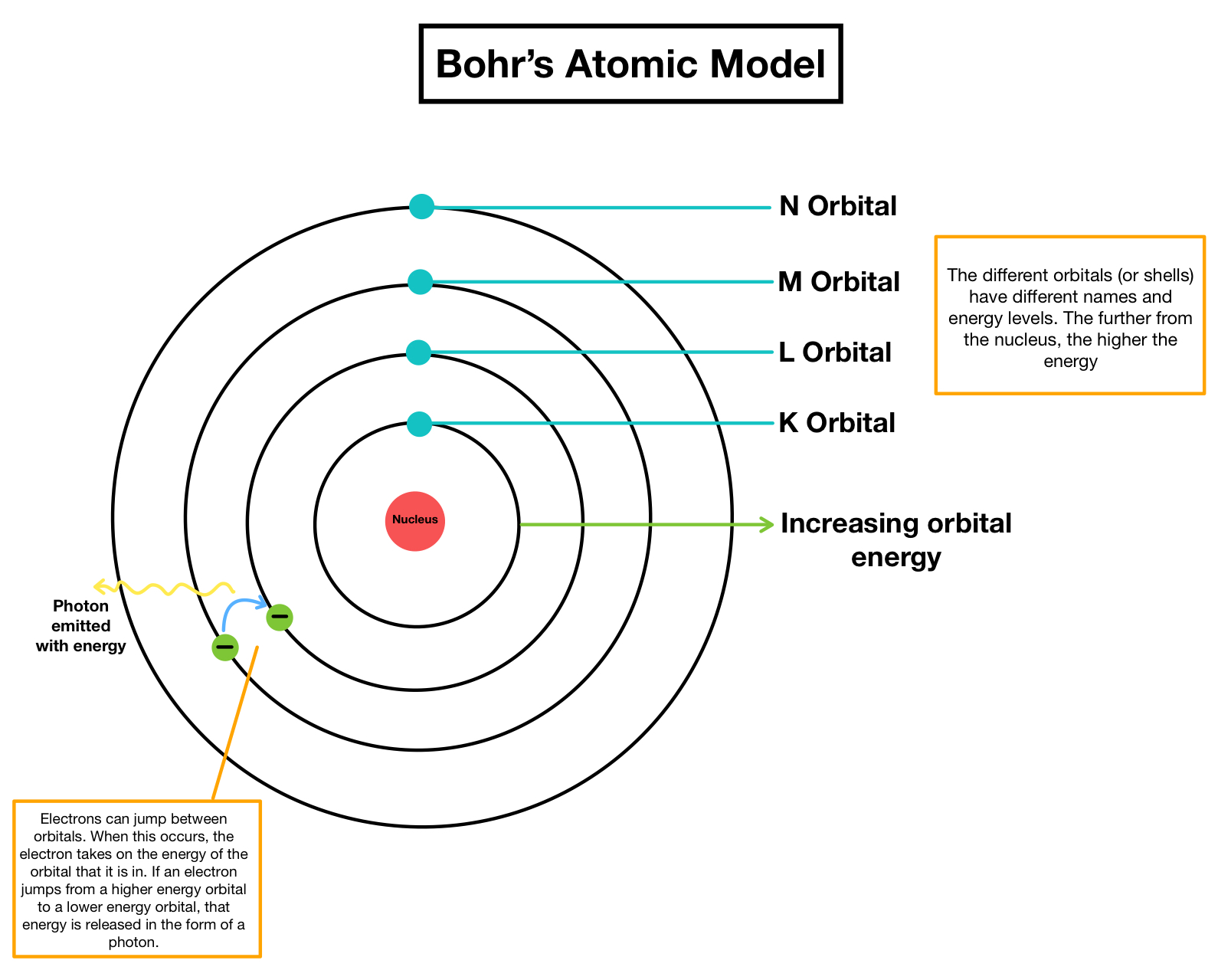
4. Энергетические уровни
Каждой орбите соответствует определённая энергия:
где
Чем дальше орбита, тем выше энергия электрона.
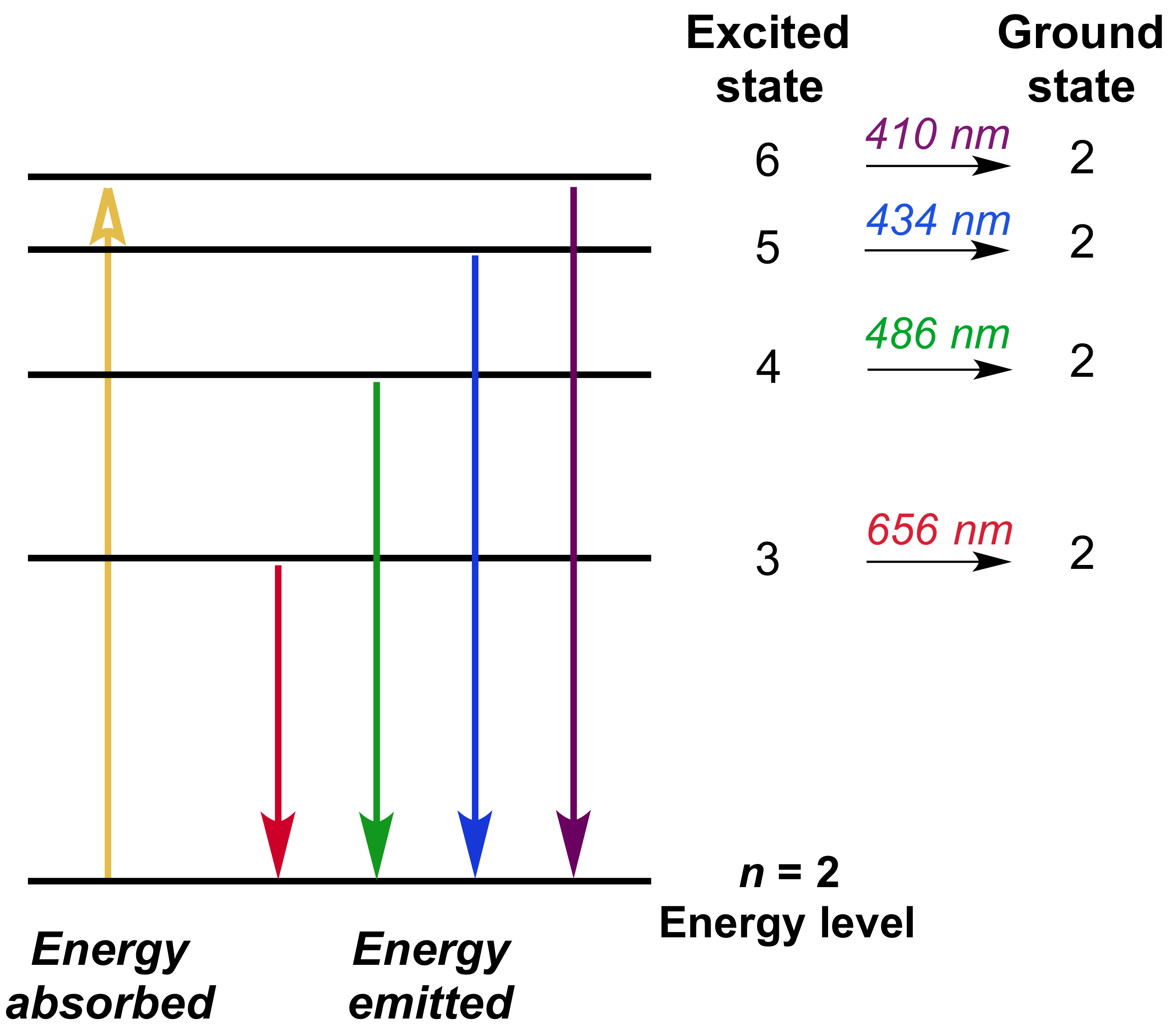
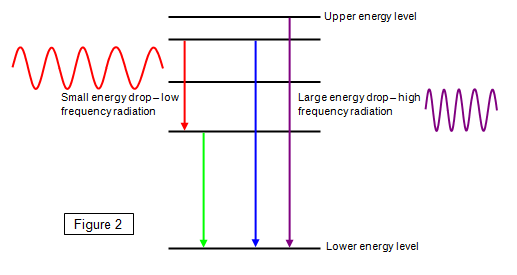
5. Излучение и поглощение света
При переходе электрона:
- с высокой орбиты на низкую → излучается фотон;
- с низкой на высокую → поглощается энергия.
Это объясняет линейчатый спектр атома водорода.
Наглядная схема переходов электрона


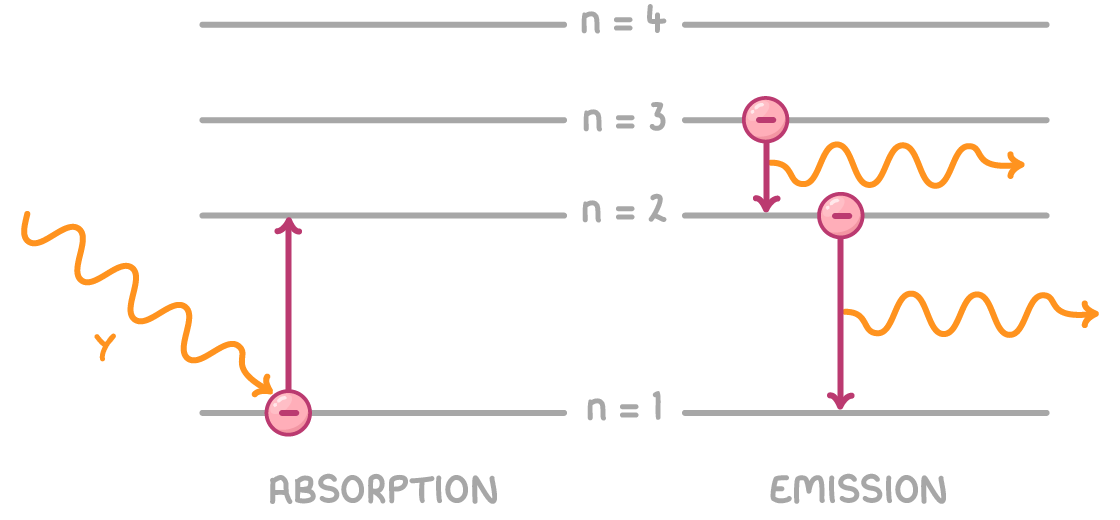
6. Значение модели Бора
-
Объяснила устойчивость атома;
-
Описала спектры водорода;
-
Ввела понятие квантования энергии;
-
Стала шагом к квантовой механике.
Однако модель работает точно только для водородоподобных атомов.
7. Итоги
-
Модель Резерфорда не могла объяснить устойчивость атома;
-
Бор ввёл квантовые орбиты;
-
Энергия электрона дискретна;
-
Переходы между уровнями сопровождаются излучением.
Вопросы для самопроверки
-
В чем суть модели Резерфорда?
-
Какие трудности возникли у этой модели?
-
Какие постулаты предложил Бор?
-
Почему электрон не падает на ядро в модели Бора?
-
Что такое энергетические уровни?
-
Как возникает линейчатый спектр?
-
В чем ограниченность модели Бора?
