Введение в химию
1. Химия как наука о веществах и их превращениях
Химия — это естественная наука, изучающая вещества, их состав, строение, свойства и превращения. Она отвечает на фундаментальные вопросы: из чего состоит окружающий мир? почему вещества ведут себя по-разному? как можно управлять их свойствами?
Любой предмет, который нас окружает — воздух, вода, металлы, пластик, ткани, продукты питания — состоит из веществ. Химия помогает понять их природу и объяснить происходящие с ними изменения.
Современная химия тесно связана с физикой, биологией, экологией, медициной и инженерией. Она лежит в основе фармацевтики, металлургии, энергетики, производства строительных материалов, косметики и бытовой химии.
2. Значение химии в жизни человека
Химия сопровождает человека на протяжении всей жизни. Даже обычные бытовые процессы имеют химическую природу.
Примеры из повседневной жизни:
-
Горение природного газа на кухне — химическая реакция окисления.
-
Ржавление железа — процесс коррозии.
-
Брожение теста — результат деятельности микроорганизмов.
-
Переваривание пищи — сложный комплекс химических реакций.
В медицине химия позволяет создавать лекарства и вакцины. В сельском хозяйстве — удобрения и средства защиты растений. В промышленности — новые материалы с заданными свойствами.
Без химии невозможно представить современное общество.
3. Понятие вещества
3.1 Что такое вещество
Вещество — это форма материи, обладающая массой и занимающая определённый объём.
Все вещества состоят из мельчайших частиц: атомов, молекул или ионов.
3.2 Физические свойства веществ
Физические свойства можно наблюдать без изменения состава вещества:
-
цвет
-
плотность
-
запах
-
температура плавления
-
температура кипения
-
растворимость
-
электропроводность
Например, вода кипит при 100 °C (при нормальном давлении), а железо имеет высокую плотность.
3.3 Химические свойства
Химические свойства проявляются при превращении одного вещества в другое:
-
горение
-
окисление
-
взаимодействие с кислотами
-
разложение при нагревании
Если железо ржавеет, оно превращается в новое вещество — оксид железа.
4. Агрегатные состояния вещества
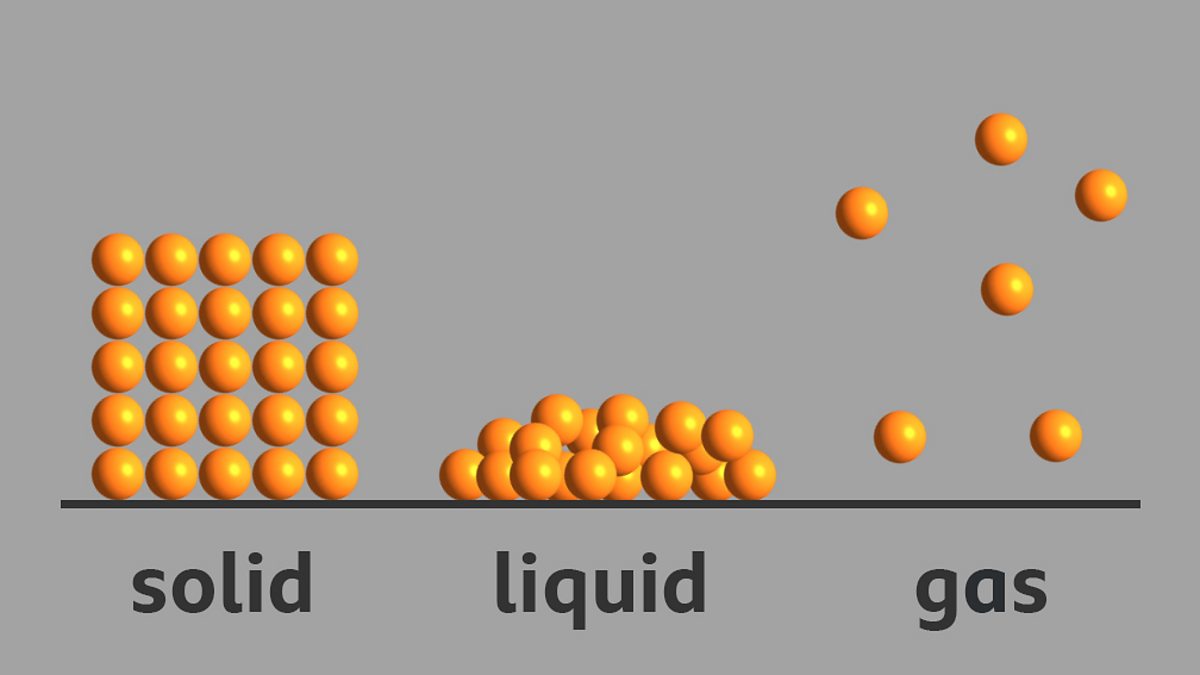

Вещества могут существовать в разных агрегатных состояниях в зависимости от температуры и давления.
4.1 Твёрдое состояние
Частицы расположены близко друг к другу и образуют упорядоченную структуру.
Примеры: лёд, соль, металлы.
4.2 Жидкое состояние
Частицы находятся близко, но могут перемещаться.
Примеры: вода, спирт, бензин.
4.3 Газообразное состояние
Частицы расположены на большом расстоянии и свободно движутся.
Примеры: кислород, азот, углекислый газ.
4.4 Плазма
Ионизированный газ, встречающийся в звёздах и молниях.
Переходы между состояниями называются фазовыми переходами: плавление, кипение, конденсация, кристаллизация.
5. Атомно-молекулярное учение
Основой современной химии является атомно-молекулярная теория.
Основные положения:
-
Все вещества состоят из атомов и молекул.
-
Атомы — наименьшие химически неделимые частицы элемента.
-
Молекулы состоят из атомов.
-
В химических реакциях атомы не исчезают и не возникают, а перераспределяются.
Эта теория позволила объяснить законы химии и развитие химической науки.
6. Строение атома
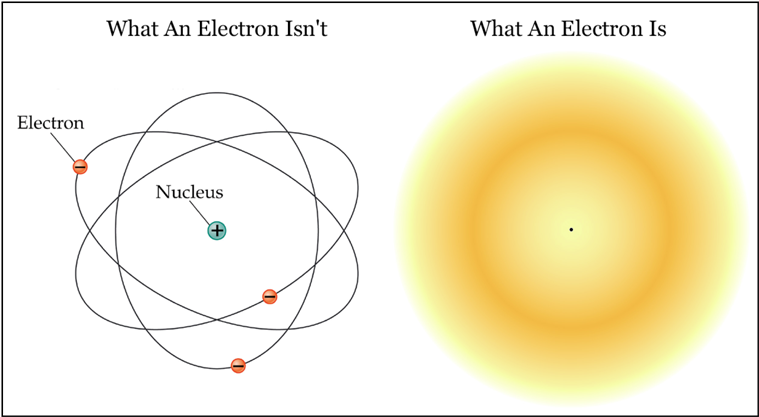
Атом состоит из двух основных частей:
-
Ядра
-
Электронной оболочки
6.1 Ядро атома
Ядро содержит:
-
протоны (положительный заряд)
-
нейтроны (без заряда)
Число протонов определяет химический элемент.
6.2 Электроны
Электроны имеют отрицательный заряд и движутся вокруг ядра. Они определяют химические свойства элемента.
7. Химические элементы
Химический элемент — это вид атомов с одинаковым числом протонов в ядре.
Например:
-
Водород (1 протон)
-
Углерод (6 протонов)
-
Кислород (8 протонов)
-
Железо (26 протонов)
Всего известно более 100 элементов.
8. Периодическая система химических элементов

Периодическая система отражает закономерности изменения свойств элементов.
Элементы расположены:
-
по возрастанию атомного номера
-
в горизонтальных рядах (периодах)
-
в вертикальных столбцах (группах)
Элементы одной группы обладают сходными химическими свойствами.
Периодическая система позволяет:
-
предсказывать свойства элементов
-
объяснять химическую активность
-
систематизировать знания о веществах
9. Простые и сложные вещества
9.1 Простые вещества
Состоят из атомов одного элемента.
Примеры: кислород (O₂), водород (H₂), железо (Fe).
9.2 Сложные вещества (соединения)
Состоят из атомов разных элементов.
Примеры: вода (H₂O), углекислый газ (CO₂), поваренная соль (NaCl).
10. Смеси и их виды
Смесь — это сочетание нескольких веществ.
10.1 Однородные смеси
Состав одинаков по всему объёму.
Пример: раствор соли в воде.
10.2 Неоднородные смеси
Компоненты можно различить.
Пример: песок и вода.
Методы разделения смесей:
-
фильтрование
-
выпаривание
-
отстаивание
-
перегонка
11. Химические реакции
Химическая реакция — это превращение одних веществ в другие.
Признаки реакции:
-
изменение цвета
-
выделение газа
-
образование осадка
-
выделение тепла
-
появление света
Типы реакций:
-
соединения
-
разложения
-
замещения
-
обмена
Химические реакции сопровождаются энергетическими изменениями.
12. Законы химии
12.1 Закон сохранения массы
Масса веществ до реакции равна массе веществ после реакции.
12.2 Закон постоянства состава
Каждое химическое соединение имеет постоянный состав.
12.3 Закон кратных отношений
Если два элемента образуют несколько соединений, массы одного элемента относятся как простые целые числа.
Эти законы стали фундаментом развития химической науки.
13. Основные разделы химии
Неорганическая химия
Изучает все элементы и их соединения, кроме большинства углеродных.
Органическая химия
Изучает соединения углерода.
Физическая химия
Изучает закономерности химических процессов.
Аналитическая химия
Определяет качественный и количественный состав веществ.
Биохимия
Изучает химические процессы в живых организмах.
14. Химия и окружающая среда
Химия помогает:
-
очищать воду
-
снижать загрязнение воздуха
-
перерабатывать отходы
-
разрабатывать экологичные материалы
Однако химические вещества могут быть опасны при неправильном использовании.
Развитие «зелёной химии» направлено на снижение вредного воздействия на природу.
15. Техника безопасности
При работе с химическими веществами необходимо:
-
использовать защитные очки
-
работать в перчатках
-
не пробовать вещества на вкус
-
соблюдать инструкции
-
не смешивать неизвестные вещества
Соблюдение правил безопасности — обязательное условие работы в лаборатории.
16. Перспективы развития химии
Современная химия развивается в направлениях:
-
нанотехнологии
-
создание новых материалов
-
альтернативная энергетика
-
фармацевтика
-
экологически безопасные технологии
Будущее химии связано с устойчивым развитием и улучшением качества жизни.
Заключение
Введение в химию позволяет понять основы устройства мира на уровне веществ и их превращений. Химия объясняет процессы, происходящие в природе и технике, и даёт человеку возможность создавать новые материалы, лекарства и источники энергии.
Изучение химии формирует научное мышление, развивает логику и умение анализировать процессы.
Вопросы для самопроверки
-
Что изучает химия?
-
Что называется веществом?
-
Назовите агрегатные состояния вещества.
-
Чем отличаются физические свойства от химических?
-
Что такое атом?
-
Из каких частиц состоит атом?
-
Что такое химический элемент?
-
В чём отличие простого вещества от сложного?
-
Какие признаки указывают на химическую реакцию?
-
Сформулируйте закон сохранения массы.
-
Почему периодическая система имеет большое значение?
-
Какие методы разделения смесей вы знаете?
-
Чем органическая химия отличается от неорганической?
-
Почему важно соблюдать технику безопасности?
-
Как химия помогает решать экологические проблемы?
