Решение задач по теме "Электрический ток в жидкостях"
1. Основные понятия
-
Электролит — жидкость, способная проводить ток благодаря наличию ионов (например, растворы соли, кислоты, щелочи).
-
Катионы — положительные ионы, движутся к катоду (отрицательный электрод).
-
Анионы — отрицательные ионы, движутся к аноду (положительный электрод).
-
Электролиз — химические реакции на электродах под действием тока.
Направление тока: условно считается от анода к катоду, хотя реальные носители заряда (катионы и анионы) движутся в противоположном направлении.
2. Закон Ома для растворов
Сила тока в растворе вычисляется по формуле:
где:
— сила тока (А),
— напряжение (В),
— сопротивление раствора (Ω), зависящее от:
- концентрации ионов;
- температуры раствора;
- расстояния между электродами;
- площади электродов.
Примечание: при увеличении концентрации ионов сопротивление уменьшается, а ток возрастает.
3. Работа и мощность тока в растворах
Работа тока за время определяется формулой:
где — работа в Джоулях,
— сила тока,
— напряжение,
— время.
Мощность тока:
Эти формулы используются для расчета энергии, затраченной на электролиз или подогрев раствора.
4. Масса вещества, выделившегося на электроде
Для электролиза используется закон Фарадея:
где:
— масса вещества, выделившегося на электроде (кг);
— заряд, прошедший через раствор (Кл);
— постоянная Фарадея (
);
— молярная масса вещества (кг/моль);
— количество электронов, участвующих в реакции.
Пример: при электролизе медного купороса ()
, так как каждый ион
принимает два электрона.
5. Наглядная схема электрического тока в жидкости
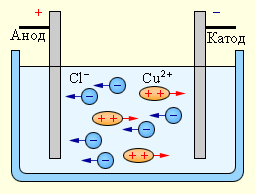

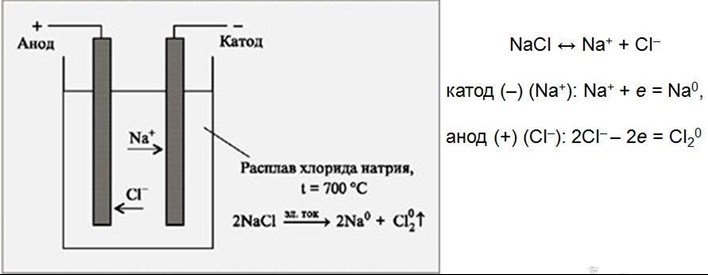
На схеме показано:
-
раствор электролита;
-
катод и анод;
-
движение катионов к катоду и анионов к аноду;
-
условное направление тока;
-
выделение вещества на электродах.
6. Пример решения задачи
Задача: Через раствор меди проходит ток
в течение
минут. Определите массу меди, осевшей на катоде.
Решение:
- Найдём заряд:
- Используем закон Фарадея:
Ответ: меди.
7. Типы задач по теме
-
Расчёт силы тока: I = U / R
-
Электролиз: масса вещества, выделившегося на электроде
-
Работа тока: A = I U t
-
Мощность тока: P = I U
-
Сопротивление раствора: по зависимости от длины, площади и концентрации ионов
8. Вопросы для самопроверки
-
Какие частицы создают ток в жидкостях?
-
Как вычислить силу тока в растворе по закону Ома?
-
Как связаны заряд, сила тока и время?
-
Как рассчитать массу вещества, выделившегося при электролизе?
-
Какие факторы влияют на сопротивление раствора?
-
Приведите пример практического применения электролиза.
-
Почему ток в растворе зависит от концентрации ионов?
