Электрический ток в жидкостях
1. Что такое ток в жидкостях
Электрический ток в жидкостях — это упорядоченное движение заряженных частиц, которыми являются ионы:
-
Положительные ионы (катионы) движутся к катоду (отрицательный электрод).
-
Отрицательные ионы (анионы) движутся к аноду (положительный электрод).
Таким образом, ток в жидкостях создаётся не электронами, как в металлах, а движением ионов.
2. Электролиты
Электролиты — это жидкости или растворы, способные проводить ток благодаря наличию ионов.
Примеры:
- Раствор соли
в воде — образует
и
.
- Раствор серной кислоты
— ионы
и
.
- Щёлочи, такие как
, дают
и
.
Неэлектролиты (например, сахарный сироп, дистиллированная вода) ток практически не проводят, так как ионов мало.
3. Механизм движения ионов
При подаче напряжения на электролит:
-
катионы движутся к катоду;
-
анионы — к аноду.
При столкновении с электродами ионы могут отдавать или принимать электроны, вызывая химические реакции. Этот процесс называется электролизом.
4. Закон Ома для электролитов
Для растворов и жидкостей закон Ома справедлив:
где — сопротивление раствора, зависящее от:
-
концентрации ионов;
-
температуры раствора;
-
расстояния между электродами;
-
площади электродов.
Чем больше концентрация ионов, тем меньше сопротивление и больше ток.
5. Наглядная схема тока в жидкостях
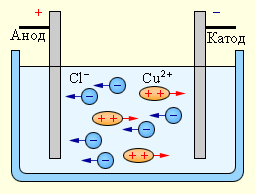
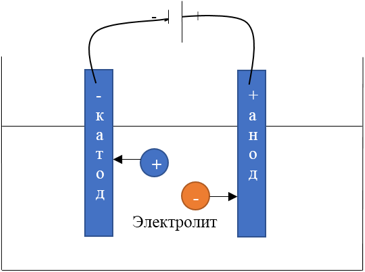
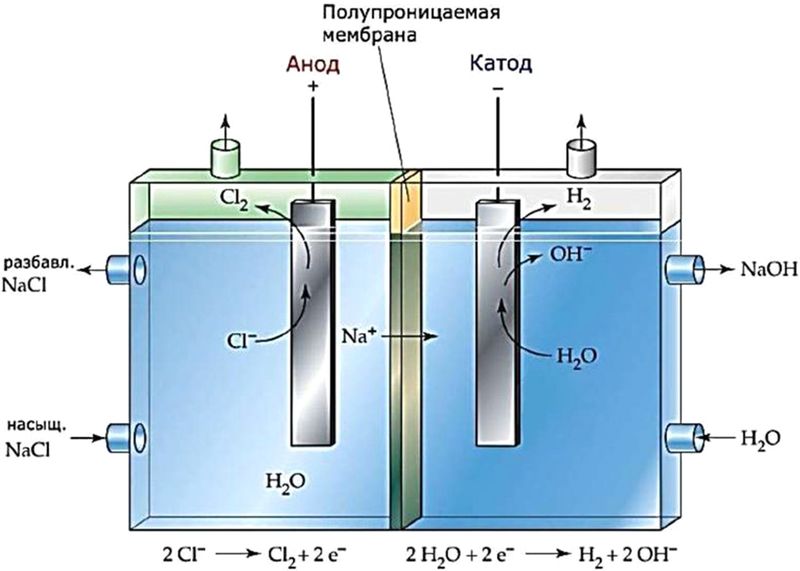
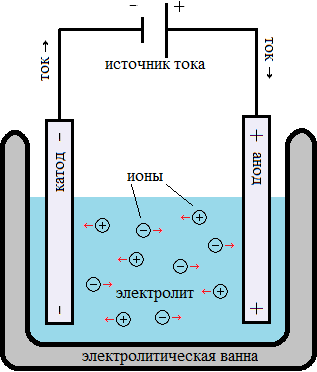
На схеме показано:
-
раствор электролита;
-
катод и анод;
-
движение катионов и анионов;
-
условное направление электрического тока.
6. Применение тока в жидкостях
-
Электролиз — разложение веществ с помощью тока.
-
Разделение воды на водород и кислород.
-
Получение металлов из растворов соли.
-
-
Аккумуляторы и батареи — ток течёт за счёт движения ионов между электродами.
-
Электрохимические датчики — определяют концентрацию веществ в растворах.
-
Гальванопластика — нанесение металла на поверхность изделия.
7. Факторы, влияющие на ток в жидкостях
-
Концентрация ионов — чем выше, тем больше ток.
-
Температура — при нагреве ток увеличивается из-за большей подвижности ионов.
-
Расстояние между электродами — чем меньше, тем меньше сопротивление.
-
Тип ионов — разная подвижность катионов и анионов.
8. Важность изучения
Знание о токе в жидкостях позволяет:
-
понимать работу аккумуляторов и батарей;
-
управлять процессами электролиза;
-
создавать датчики и химические приборы;
-
изучать реакции на электродах.
9. Вопросы для самопроверки
-
Какие частицы создают ток в жидкостях?
-
Чем электролиты отличаются от неэлектролитов?
-
Как движутся катионы и анионы в растворе?
-
Что такое электролиз?
-
Какие факторы влияют на сопротивление раствора?
-
Приведите примеры применения электрического тока в жидкостях.
-
Почему дистиллированная вода плохо проводит ток?
